
ANNIE TALBOT, RANIA KHEMIRI, AÏSSATE SAKO, LUC LONDEI-LEDUC, CHRISTINE ROBIN, SUZANNE MARCOTTE, GUENIÈVRE THERRIEN, GENEVIÈVE GOULET, GENEVIÈVE BEAUDET HILLMAN, CHRISTINE OUELLETTE, SUZANNE BRISSETTE, MARCEL MARTIN, POLINA TITOVA, PIERRE LAUZON/
Annie Talbot, chercheuse, médecin, Centre de recherche du Centre hospitalier de l’Université de Montréal
Rania Khemiri, coordonnatrice de recherche, Centre de recherche du Centre hospitalier de l’Université de Montréal
Aïssata Sako, directrice de programme, Centre de recherche du Centre hospitalier de l’Université de Montréal
Luc Londei-Leduc, médecin, Centre hospitalier de l’Université de Montréal
Christine Robin, médecin, Centre intégré universitaire de santé et des services sociaux de l’Estrie – CHUS
Suzanne Marcotte, pharmacienne, Centre hospitalier de l’Université de Montréal
Guenièvre Therrien, médecin, Hôpital Notre-Dame du Centre intégré universitaire de santé et des services sociaux du Centre-Sud-de-l’Île-de-Montréal
Geneviève Goulet, médecin, Centre intégré universitaire de santé et des services sociaux de l’Estrie – CHUS
Geneviève Beaudet Hillman, infirmière clinicienne, Centre hospitalier de l’Université de Montréal
Christine Ouellette, médecin, Centre intégré universitaire de santé et des services sociaux de l’Est-de-l’Île-de-Montréal
Suzanne Brissette, chercheuse, médecin, Centre de recherche du Centre hospitalier de l’Université de Montréal
Marcel Martin, médecin, Hôpital Notre-Dame du Centre intégré universitaire de santé et des services sociaux du Centre-Sud-de-l’Île-de-Montréal
Polina Titova, coordonnatrice de recherche, Centre de recherche du Centre hospitalier de l’Université de Montréal
Pierre Lauzon, médecin, Hôpital Notre-Dame du Centre intégré universitaire de santé et des services sociaux du Centre-Sud-de-l’Île-de-Montréal
Correspondance
Annie Talbot
Centre de recherche du Centre Hospitalier de l’Université de Montréal
850, rue Saint-Denis, bureau S344
Montréal (Québec) Canada H2X 0A9
Téléphone : 514 890-8000, poste 13043
annie.talbot.md.chum@ssss.gouv.qc.ca
Remerciements
Nous tenons à remercier tous les patients et le personnel soignant qui a collaboré au projet
SuboxED, notamment mesdames Karell Bossé, Hélène Loiselle, Sylvie Hall et monsieur Sofiane Chougar. Nous voulons également remercier la Dre Julie Bruneau et le pôle Québec-Atlantique de l’Initiative canadienne de recherche sur l’abus de substances (ICRAS) ainsi que l’Institut universitaire sur les dépendances pour leur soutien.
Financement
L’étude a été financée par Santé Canada et le MSSS/Institut universitaire sur les dépendances (IUD) dans le cadre du Programme sur l’usage et les dépendances aux substances. Notez que les opinions exprimées dans la présente publication ne reflètent pas nécessairement la position de Santé Canada et du MSSS.
Divulgation de conflits d’intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts à divulguer. Un membre de la famille d’Annie Talbot travaille dans une entreprise pharmaceutique (sans aucun lien avec le projet SuboxED).
Résumé
Contexte : Entre janvier 2016 et juin 2020, le Canada a enregistré plus de 17 602 décès attribuables à des cas de surdose aux opioïdes ; une hausse inquiétante qui incite les professionnels de la santé à réfléchir à des interventions dans les salles d’urgence (SU) qui sont souvent la première ligne de soins pour les personnes à risque de surdose aux opioïdes (RSO).
En avril 2018, un groupe pluridisciplinaire de cliniciens a développé le projet SuboxED pour établir un processus de mise en œuvre d’un algorithme clinique pour la distribution de naloxone intranasale pour les patients à RSO et la prescription de buprénorphine-naloxone (B/n) dans trois SU du Québec pour les patients ayant un trouble de l’usage d’opioïdes (TUO).
Méthodologie : Le projet SuboxED se présente en deux phases, la phase pré et mise en œuvre et la phase d’évaluation clinique. Nous traiterons ici de la première phase qui s’est déroulée du 1er avril 2018 au 30 avril 2019 par un processus conçu en plusieurs étapes progressives : 1) constituer un groupe pluridisciplinaire de cliniciens ; 2) identifier trois SU, des cliniques TAO et les pharmacies partenaires au Québec ; 3) établir les critères d’éligibilité à la naloxone intranasale et la B/n basée sur les recommandations scientifiques pour créer l’algorithme ; 4) former le personnel des SU ; 5) mettre en œuvre l’algorithme pour les patients RSO.
Conclusion : Le projet SuboxED a développé un algorithme clinique en réponse à la crise des opioïdes au Québec et a contribué à la gratuité de la naloxone, tout en relevant de nombreux défis. La mise en œuvre de tel algorithme est faisable et devrait être déployée largement surtout en temps de pandémie. Une phase de l’évaluation clinique suivra.
Mots-clés : buprénorphine-naloxone, naloxone, algorithme, salle d’urgence, opioïdes, surdose
An algorithm of care as a response to the opioid crisis
Abstract
Between January 2016 and June 2020, Canada recorded more than 17,602 deaths attributable to opioid overdose, an increase that prompts healthcare professionals to develop clinical interventions aimed at decreasing population overdose. As emergency departments (EDs) are often the first point of care for people at risk of opioid overdose, the current intervention focused on dispensing take-home naloxone (THN) and initiating opioid agonist treatment (OAT) among ED patients who are at risk of opioid overdose (ROO). In 2018, the SuboxED project convened a multidisciplinary group of clinical experts to implement a clinical algorithm for dispensing THN and prescribing buprenorphine/naloxone (B/n) for at ROO patients in 3 Québec EDs.
Methodology: This project had two phases: 1) planning and implementation, and 2) evaluation. This article will describe the first phase, from April 1, 2018 to April 30, 2019, which included several progressive stages: 1) convening a multidisciplinary group of clinicians ; 2) identifying the EDs, OAT clinics, and pharmacy partnerships in Quebec ; 3) establishing the eligibility criteria for intranasal naloxone and B/n based on scientific recommendations ; 4) developing training tools and the ED algorithm ; and 5) implementing the algorithm for patients at ROO.
Conclusion: The SuboxED project developed a clinical algorithm in response to the opioid crisis in Quebec and contributed to improving naloxone access in EDs, despite many challenges. The implementation of such an algorithm is feasible and should be deployed widely, especially during health crises such as the COVID-19 pandemic. The clinical evaluation of the implementation process will follow.
Keywords: buprenorphine/naloxone, take-home naloxone, emergency room, overdose,
opioid, algorithm
Implementación de un algoritmo de asistencia en respuesta a la crisis de los opioides
Resumen
Contexto: entre enero de 2016 y junio de 2020 Canadá registró más de 17 602 casos de muertes atribuibles a casos de sobredosis de opioides, un aumento inquietante que incita a los profesionales de la salud a considerar las intervenciones que se pueden realizar en las salas de emergencia para disminuir los riesgos de sobredosis, puesto que las emergencias están a menudo en la primera línea de la atención médica en los casos de personas a riesgo de sobredosis de opioides.
En abril de 2018, un grupo multidisciplinario de personal médico desarrolló el proyecto SuboxED para establecer un proceso de puesta en práctica de un algoritmo clínico para la distribución de naloxona intranasal para los pacientes con riesgo de sobredosis de opioides y de la prescripción de buprenorfina-naloxona (B-n) en tres salas de emergencia de Quebec destinada a los pacientes que presentan un problema de consumo de opioides.
Metodología: el proyecto SuboxED se presenta en dos etapas, la etapa previa a la implementación y la implementación y la etapa evaluación clínica de la implementación. Trataremos aquí la primera etapa que se ha aplicado del 1 de abril de 22018 al 30 de abril de 2019 por medio de un proceso concebido en varias etapas progresivas: 1) constituir un grupo multidisciplinario de personal médico ; 2) identificar tres salas de emergencia, las clínicas para pacientes que presentan problemas de consumo de drogas y las farmacias asociadas de Quebec ; 3) establecer los criterios de elegibilidad para la naloxona intranasal y la B-n sobre la base de las recomendaciones científicas para crear el algoritmo ; 4) formar el personal de las salas de emergencia ; 5) implementar el algoritmo para los pacientes a riesgo de una sobredosis por opioides.
Conclusión: el proyecto SuboxED ha desarrollado un algoritmo clínico en respuesta a la crisis de los opioides en Quebec y ha contribuido a la gratuidad de la naloxona, debiendo enfrentar al mismo tiempo una cantidad de desafíos. La aplicación del algoritmo es factible y debería implementarse ampliamente, sobre todo en época de pandemia. Se realizará posteriormente una etapa de evaluación clínica.
Palabras clave: buprenorfina-naloxona, naloxona, algoritmo, sala de emergencia, opioides, sobredosis.
Introduction
L’Amérique du Nord s’est retrouvée confrontée à une augmentation dramatique des décès par surdose aux opioïdes, liée, entre autres, à l’usage médical abondant des opioïdes prescrits pour soulager les douleurs (National Center for Health Statistics, 2021). La disponibilité de ces substances a facilité leur usage à des fins non médicales et proscrites. Les rapports du Centers for Disease Control and Prevention (CDC) déclaraient plus de 47 000 décès de surdose aux opioïdes au cours de l’année en 2018 aux États-Unis (CDC, 2019). Le Canada, deuxième pays au palmarès de la consommation d’opioïdes prescrit par habitant derrière les États-Unis, a enregistré entre janvier 2016 et juin 2020 une augmentation du nombre de surdoses fatales reliée aux opioïdes illicites ou prescrits (Commission globale des politiques en matière de drogues, 2018). Le gouvernement du Canada a publié un rapport en 2020 qui évalue à plus de 17 602 le nombre de décès attribuables à une intoxication aux opioïdes durant cette période. Une tendance à la hausse a aussi été observée pour le Québec
avec 258 décès en 2016, 203 décès en 2107, 280 décès en 2018 et 643 décès entre juillet 2019 à septembre 2020 (Agence de la santé publique du Canada, 2020).
L’augmentation du nombre de prescriptions des opioïdes pour des douleurs chroniques non cancéreuses, l’utilisation à des fins non thérapeutiques et la disponibilité des opioïdes illicites comme le fentanyl sur le marché serait à l’origine des cas de surdose aux opioïdes (Scholl et al., 2017).
Population à risque
Le risque de décès par surdose aux opioïdes est plus élevé chez les personnes ayant un trouble d’usage d’opioïdes (TUO) qui sont momentanément sevrées après une incarcération ou un séjour hospitalier (Merrall et al., 2010).
En Ontario, une autre étude révèle que des surdoses mortelles ont eu lieu principalement chez des personnes qui avaient déjà reçu une ordonnance d’opioïdes dans les quatre semaines précédentes ou une prescription d’opioïdes à longue action ou à forte dose (Dhalla et al., 2009).
Les salles d’urgence : première ligne de front
Au-delà des visites aux SU pour surdose aux opioïdes, les SU sont sur la ligne de front lorsque vient le temps d’évaluer les patients à risque de surdose aux opioïdes (RSO) vu les différentes raisons qui amènent les patients à consulter (épisode de soins aigus nécessitant une prescription d’opioïdes, intoxications, aide en situation de sevrage, soulagement de la douleur chronique, association médicamenteuse, comorbidités et usage opioïdes, etc.).
Weiner et ses collaborateurs (2020) ont mené une étude rétrospective de 2011 à 2015 au Massachusetts (États-Unis), sur un échantillon de 17 241 patients ayant quitté les SU après une surdose d’opioïde non mortelle. Cette étude rapporte un taux de mortalité de plus de 5,0 % pour les patients au courant de l’année suivant une surdose. Leece et ses collaborateurs (2020) ont étudié l’incidence et les facteurs de risque de mortalité auprès d’une cohorte de 6 140 patients en Ontario (Canada) entre janvier 2015 et 31 décembre 2016. Cette étude montre que 1,9 % des patients ont succombé à une surdose d’opioïdes l’année suivant leur séjour aux SU. Ils ont alors conclu à la nécessité de déployer un traitement adéquat et opportun dans les SU afin de prévenir d’éventuel cas de mortalité.
Certains patients à RSO qui visitent les SU sont des clientèles vulnérables qui sont désaffiliées du réseau de la santé. Leur seul contact avec le système de santé n’est que par des visites aux SU (Hoffman et al., 2019).
Naloxone : antidote aux surdoses d’opioïdes
Depuis 2014, l’Organisation mondiale de la Santé (OMS) préconise une meilleure accessibilité à la naloxone pour les personnes à RSO et leur entourage afin de prévenir les décès. La naloxone est un antagoniste à courte demi-vie des récepteurs opioïdes. Elle est un antidote efficace en cas de surdose pour renverser l’effet dépresseur sur les voies respiratoires et ainsi éviter un décès (OMS, 2014).
Historique de l’accès à la naloxone au Québec
Au Québec, depuis plus de quarante ans, la naloxone, sous sa forme intramusculaire ou intraveineuse, est utilisée par les professionnels de la santé pour des patients en surdose aux opioïdes dans les cliniques ou dans les centres de santé incluant les centres hospitaliers (CH). L’utilisation de la naloxone à emporter pour les personnes à RSO et leur entourage n’était pas encore disponible avant les années 2010. En 2013, à la suite d’une hausse des surdoses aux opioïdes à Montréal, le projet PROFAN (Prévenir et Réduire les Overdoses, Former et Accéder à la Naloxone) a vu le jour et a permis de faciliter l’accès à la naloxone à emporter et la remise de trousses de naloxone sous la forme intramusculaire (aiguilles, gants et instructions) aux personnes à RSO et leur entourage pour un usage hors milieu clinique. PROFAN a aussi créé des ateliers de formations par et pour les usagers de drogues et leur entourage sur la prévention des surdoses aux opioïdes et l’utilisation de la naloxone à emporter (CRAN, 2021).
En 2017, le gouvernement québécois a voulu améliorer l’accès à la naloxone aux personnes à RSO et leur entourage en mettant sur pied un programme universel gratuit géré par la Régie de l’assurance maladie du Québec (RAMQ) de distribution de la naloxone à emporter, en administration intramusculaire dans un premier temps, sous forme d’ordonnance collective puis en pharmacie d’office et sans ordonnance, pour finalement inclure, dans un deuxième temps, la forme d’administration intranasale de la naloxone une fois commercialisée au Québec. Toutefois, le programme n’incluait pas la remise de la naloxone à emporter dans les SU des centres hospitaliers (Institut national de santé publique du Québec [INSPQ], 2017).
Trouble d’usage d’opioïdes : la buprénophine/naloxone comme traitement de première ligne
Une composante déterminante chez les patients à RSO est le TUO. Ainsi, au-delà de la prévention d’un décès par surdose aux opioïdes à la suite de l’administration de la naloxone, les patients avec un TUO peuvent aussi nécessiter un traitement par agoniste aux opioïdes (TAO) afin de réduire les risques de surdoses, les infections associées à l’utilisation des opioïdes
et de diminuer la criminalité (Bruneau et al., 2018). La buprénorphine/naloxone (B/n), un des TAO disponibles sur le marché, est une association médicamenteuse de deux ingrédients actifs (la buprénorphine et la naloxone). La buprénorphine est un agoniste partiel des récepteurs opioïdes qui, par son action agoniste, supprime l’effet de sevrage, réduit les effets sur le système respiratoire et les risques de dépression respiratoire dû à une surdose. Elle est disponible sous la forme de comprimé sublingual (Stotts et al., 2009). La naloxone est ajoutée à sa composition pour éviter une surdose de buprénorphine par injection, et n’est pas active dans la forme sublinguale (Harris et al., 2000 ; Mendelson et al., 1997). La B/n prévient donc les symptômes de sevrage d’opioïdes et diminue le désir de consommer des opioïdes.
Selon les lignes directrices nationales de l’Initiative canadienne de recherche en abus de aubstance (ICRAS), la B/n est considérée comme traitement de première ligne chez les patients ayant un TUO (Bruneau et al., 2018). Par ailleurs d’autres études soulignent les avantages économiques d’une induction à la B/n aux SU pour le système de santé comparativement à une psychothérapie de type intervention brève ou une référence dans un centre spécialisé en toxicomanie (Busch et al., 2017). Le mot induction à la B/n est utilisé dans ce texte comme synonyme d’initiation ou amorce à la B/n.
La buprénorphine/naloxone aux salles d’urgence
L’étude de 2017 de D’Onofrio et ses collaborateurs portent sur les patients avec un TUO ayant été initié à la B/n aux SU. Les données de cet essai clinique randomisé ont montré que 74,0 % des patients des groupes de randomisation à la B/n avaient une meilleure rétention dans leur traitement que ceux du groupe qui ont été référés à une clinique TAO. De plus, les auteurs de cette étude confirment que les patients du groupe B/n rapportent une diminution significative de leur consommation d’opioïde deux mois après l’amorce de la B/n aux SU. Ces effets n’ont cependant pas pu être observés six mois plus tard (D’Onofrio et al., 2017).
À la suite de la publication des résultats de cette étude et devant l’ampleur de la crise des surdoses aux opioïdes, des cliniciens américains aux États-Unis ont mis en place des programmes aux SU pour l’induction de la B/n chez les personnes ayant un TUO (Siegel, 2019). Au Canada (Alberta et Ontario), un programme de remise de trousse de naloxone a été mis en place dans l’hôpital urbain tertiaire Royal Alexandra à Edmonton (O’Brien et al., 2019), toutefois, sans amorce de la B/n chez les personnes ayant un TUO aux SU.
SuboxED : la genèse
En décembre 2017, pour endiguer cette urgence sanitaire, le projet SuboxED a été élaboré au Québec. Ce projet, subventionné par le Programme sur l’usage et les dépendances aux substances (PUDS) qui vise à appuyer les initiatives novatrices en promotion de la santé, en prévention et réduction des méfaits, s’arrime aux plans d’action du ministère de la Santé et des Services sociaux (MSSS) pour faire face à la crise des opioïdes (MSSS, 2018).
Objectifs
Le projet SuboxED vise la création et la mise en œuvre de l’algorithme de la naloxone intranasale à des patients à RSO, l’amorce de la B/n chez les patients ayant un TUO identifié dès la SU et l’évaluation clinique six mois après la mise en œuvre de cet algorithme.
Nous décrivons dans cet article les étapes de la mise en œuvre de cet algorithme dans trois SU au Québec.
Éthique
Le protocole de recherche du projet SuboxED été évalué par le comité scientifique du CHUM, ensuite approuvé par le comité d’éthique de recherche (CER) du CHUM, désigné CER évaluateur du projet. Par la suite, les autorisations de poursuivre la recherche ont été sollicitées et obtenues auprès des comités d’éthique affiliés aux SU impliquées.
Méthodologie
Description de la stratégie de la mise en œuvre
Sélection des trois SU participantes
Le projet SuboxED s’est déroulé du 3 décembre 2017 au 31 mars 2020 et a été mené au sein de trois SU du Québec (figure 1). Les trois SU sélectionnées sont : 1) le Centre hospitalier de l’Université de Montréal (CHUM), un hôpital universitaire de Montréal en plein cœur du centre-ville de Montréal, offrant des services hautement spécialisés avec une estimation de 75 000 visites annuelles à la SU avec des équipes spécialisées en médecine des toxicomanies, disponible par consultations, 24 heures par jour, sept jours semaine (CHUM, 2019). On estime qu’environ 1 500 consultations sont effectuées au Service de la médecine des toxicomanies (SMT) en provenance de la SU ; 2) l’hôpital Notre-Dame du Centre intégré universitaire de santé et des services sociaux (CIUSSS) du Centre-Sud-de-l’Île-de-Montréal, un hôpital de quartier de Montréal dont les activités cliniques sont centrées sur la médecine de proximité avec une estimation de 47 000 visites annuelles qui ont également accès à des équipes spécialisées en médecine des toxicomanies sur consultations, 24 heures par jour, sept jours semaine (Hôpital Notre-Dame du CIUSSS du Centre-Sud-de-l’Île-de-Montréal, 2019). On estime qu’environ 1 000 consultations sont effectuées au Service des toxicomanies et de médecine urbaine (STMU) en provenance de la SU ; et 3) l’hôpital Hôtel Dieu du CIUSSS de l’Estrie-CHUS, situé au centre-ville de Sherbrooke, avec une estimation de 51 000 visites annuelles qui a accès aux services ambulatoires par référence du centre de réadaptation en dépendance du CIUSSS de l’Estrie-CHUS, cinq jours par semaine entre 8 h et 17h. On estime qu’environ 87 références sont effectuées au centre de réadaptation en dépendance du CIUSSS de l’Estrie-CHUS (Hôpital Hotel Dieu du CIUSSS de l’Estrie-CHUS, 2019).
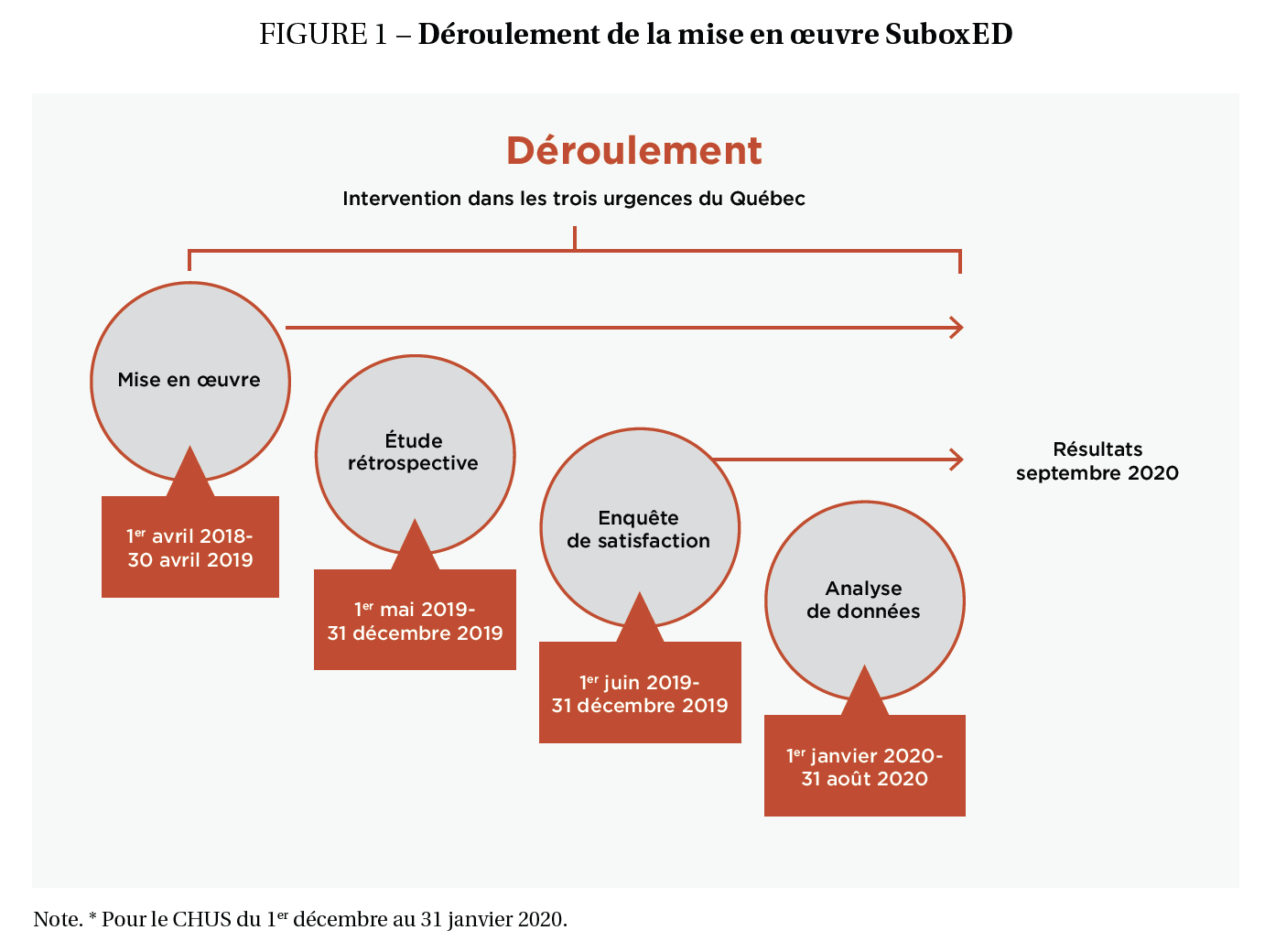
Ces trois salles d’urgence ont été sélectionnées selon les critères suivants : 1) la volumétrie de leur clientèle, la diversité des patients reçus pour des intoxications, surdoses et autres affections liées à la consommation de substances, et les différences dans les soins et services offerts ; 2) la capacité et la volonté des équipes cliniques et de gestion des services d’urgences à intégrer rapidement un nouvel algorithme ; 3) la disponibilité de toutes les ressources matérielles, humaines, départementales et financières pour la mise en œuvre de SuboxED.
Sélection du groupe de cliniciens pluridisciplinaires
Un groupe de cliniciens pluridisciplinaires composés de pharmaciens d’hôpitaux, de médecins à l’urgence, de médecins ayant une expertise en toxicomanie, de résidents, d’infirmières en soins d’urgence et en toxicomanie ainsi que de gestionnaires d’hôpitaux a été formé. Préoccupés par la crise des opioïdes au sein des trois SU sélectionnés, ils ont décidé de mettre en commun leurs connaissances en soins d’urgence et en médecine des toxicomanies afin de développer et mettre en place un algorithme de distribution de la naloxone intranasale et de prescription de B/n au sein de ces SU pour les patients à RSO ou ayant un TUO.
De mars 2018 à avril 2019, ce groupe de cliniciens pluridisciplinaires s’est réunis une fois par mois pour : 1) réviser la revue de littérature ; 2) élaborer l’algorithme de dispensation de la naloxone et de prescription la B/n aux SU basée sur cette littérature ; 3) créer des liens avec trois cliniques de TAO affiliées à chaque SU ; 4) identifier les pharmacies d’officines partenaires ; 5) s’assurer de l’accès à la naloxone intranasale et de la B/n dans les SU ; 6) développer des outils cliniques propres à la mise en œuvre de l’algorithme ; 7) discuter des enjeux de mise en œuvre propres à chacune des SU ; 8) résoudre les enjeux découlant dans la mise en œuvre ; 9) cibler les formations nécessaires ; 10) créer le contenu de formation ; 11) répondre aux questions des équipes terrain des trois SU en lien avec la mise en œuvre (formation, outils, aspect clinique, etc.).
Le groupe de cliniciens pluridisciplinaires a travaillé conjointement avec les directions des soins infirmiers de chaque établissement de santé des trois SU, les pharmaciens d’officine, les pharmaciens des SU et les médecins à l’urgence des trois SU pour développer des plans de formation pour les équipes impliquées.
Sélection et rôles des trois cliniques TAO
Le Service de médecine des toxicomanies (SMT) du CHUM, le Service des toxicomanies et de médecine urbaine (STMU) de l’hôpital Notre-Dame du CIUSSS et la clinique externe de TAO du CIUSSS de l’Estrie-CHUS – établissement Centre Jean-Patrice-Chiasson, sont les cliniques TAO des trois sites où s’est déroulée la mise en œuvre du projet SuboxED. Les trois cliniques TAO ont été choisies selon la proximité aux SU et leur capacité à évaluer les patients initiés à la B/n aux SU dans un délai sept jours ou moins.
Ces collaborations ont permis de développer les processus de référence et de prise en charge des patients après leur congé des SU dans les trois cliniques TAO.
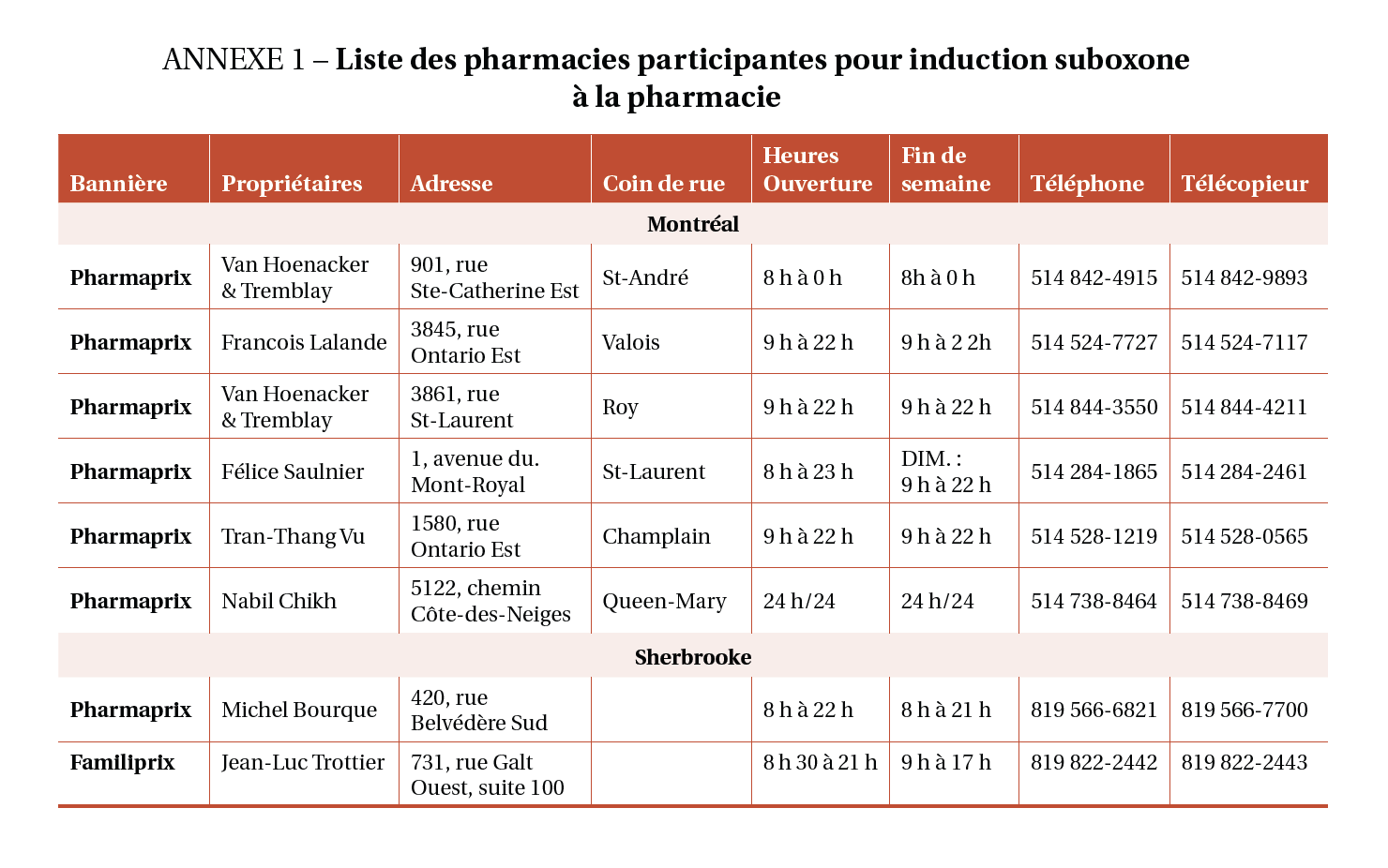
Sélection des huit pharmacies d’officine
Les huit pharmacies d’officine ont été sélectionnées selon leur expertise en TAO (induire en totalité ou partiellement, la B/n à leur pharmacie) et selon leur proximité démographique en lien avec les SU ainsi que les heures d’ouverture. Cette collaboration consistait à : 1) faciliter le transfert des patients après leur congé de l’urgence et leur prise en charge subséquente ; 2) l’amorce de la B/n en pharmacie, lorsque prescrite ; 3) la remise et l’ajustement du dosage de la prescription de la B/n ainsi que la remise de naloxone intranasale par le pharmacien d’officine, lorsqu’indiqué (annexe 1).
Identification de la population cible
La population ciblée par le projet SuboxED est constituée des personnes qui visitent les SU et qui sont identifiées à RSO par les professionnels de la santé des SU.
Le groupe de cliniciens pluridisciplinaires a proposé une question unique d’identification des patients à RSO aux SU s’intégrant parfaitement au questionnaire de triage déjà existant des infirmières (figure 3), selon les définitions de l’OMS, CDC et INSPQ (OMS, 2014 ; CDC, 2019 ; INSPQ, 2017). De plus, il a été établi pour chacune des trois SU, que le dépistage
des personnes à RSO se faisait soit par l’infirmière de triage, l’infirmière aux soins du patient ou par le pharmacien de la SU.

Algorithme de soins pour la distribution de naloxone intranasale et l’induction de la B/n
Lors des rencontres préparatoires de la mise en œuvre, les médecins des SU ont mentionné le besoin de développer des outils d’identification des patients à RSO simple et facile à mettre en pratique comme c’est le cas des ordonnances préimprimées qui permettent une prise en charge sécuritaire et un algorithme en réponse aux besoins des patients à RSO ou TUO sans toutefois prolonger leur séjour aux urgences de façon inutile. Ces commentaires ont été pris en considération dans la création des outils.
Ainsi, les cliniciens pluridisciplinaires, aidés par la revue de littérature, ont élaboré un algorithme de soins décisionnel pour la remise de la naloxone intranasale chez les patients à RSO et la prescription de B/n pour les patients ayant un TUO, qui inclut l’identification du patient à RSO, la remise de la naloxone et la prescription de B/n.
Tous les outils cliniques ont été révisés et approuvés par les instances incluant la direction des soins infirmiers, les comités des dossiers cliniques pour l’ajout d’outils cliniques dans les dossiers médicaux et les comités des pharmaciens des établissements respectifs.
Critères d’éligibilité des patients à la naloxone intranasale
Pour déterminer si un patient à RSO doit recevoir la naloxone intranasale, un outil clinique a été développé selon les critères établis par l’équipe pluridisciplinaire, basée sur les recommandations des lignes directrices de l’Institut national d’excellence en santé et services sociaux (INESSS), l’Institut national de santé publique du Québec (INSPQ), le CDC et l’OMS (CDC, 2019 ; INESSS, 2018 ; INSPQ, 2017 ; OMS, 2014).
Des critères d’exclusion de remise de la naloxone ont aussi été intégrés (figure3).

Critères d’éligibilité des patients à la B/n
Un outil clinique a été développé pour les médecins des SU afin de déterminer les critères d’éligibilité des patients à la B/n et la confirmation d’un diagnostic de TUO selon la cinquième version du Manuel diagnostique et statistique des troubles mentaux (DSM-5 ; American Psychiatric Association, 2013), et les recommandations du Collège des médecins et de l’Ordre des pharmaciens du Québec (Collège des médecins du Québec et al., 2020).
Les critères d’admissibilité pour une induction sont les suivantes :
- le patient doit avoir un diagnostic de dépendance selon le DSM-5 ou un comportement qui risque de mettre sa vie en danger ;
- le patient doit être âgé de plus de 14 ans ;
- le patient doit avoir un historique de consommation importante d’opioïdes et plusieurs tentatives de sevrage ;
- le patient doit consommer des opioïdes (confirmation par test urinaire ou historique médicale) ;
- et finalement, le patient doit pouvoir consentir et accepter les soins.
Les doses retenues d’induction de B/n, l’ajustement suggéré, la gestion des sevrages provoqués et les prescriptions types pour les pharmacies d’officines respectent à la fois les règles du Collège des médecins et de l’Ordre des pharmaciens du Québec (Collège des médecins du Québec et al., 2020), en plus de respecter les propriétés pharmaceutiques de la B/n.
Formation du personnel des trois SU
Le programme de formation du projet SuboxED pour le personnel des SU, des pharmaciens d’officines et les professionnels des cliniques TAO portait sur la naloxone, la B/n et l’algorithme développé. Ce programme contenait deux types de formations : 1) deux modules de formation en ligne ; et 2) sessions d’échange sur la mise en œuvre de l’algorithme.
Lors des rencontres préparatoires de formation, les professionnels de la santé rencontrés ont mentionné le besoin de développer des outils de formation virtuelle afin de cibler tous les quarts de travail des SU et des pharmacies d’officines, des sessions de questions-réponses et du temps rémunéré libéré pour les formations des infirmières.
Modules de formation
Des infirmières et des médecins spécialisés en médecine des toxicomanies du CHUM, responsables de la formation, ont préparé deux modules de formation virtuelle de 20 minutes chacun. Le premier module porte sur l’utilisation de l’échelle Clinical Opioid Withdrawal Scale (COWS) (annexe 5). Cette échelle de 11 items permet l’évaluation des symptômes de sevrage aux opioïdes en combinant des symptômes subjectifs et objectifs observés chez le patient. Elle est conçue pour être utilisée rapidement (< deux minutes) par les cliniciens. L’échelle et son pointage limitent la possibilité de réponses feintes (Wesson et Ling, 2003). Cet outil est un instrument valide et présente une sensibilité suffisante pour détecter un sevrage aux opioïdes (Tompkins et al., 2009).
La COWS est couramment utilisée pour l’induction à la buprénorphine ou à la B/n, mais peut également être utilisée dans l’évaluation du sevrage aigu des opioïdes dans d’autres contextes, comme le traitement TAO à la méthadone et le traitement de la douleur chronique.
Le deuxième module porte sur les critères de dispensation de la naloxone à emporter à partir d’un centre hospitalier pour les patients à RSO pour usage hors milieu clinique. Ces modules ont été spécialement conçus pour le personnel des SU et fournissent des informations générales sur l’utilisation de la naloxone, les facteurs de risque de surdose, ainsi que les signes et symptômes du sevrage des opioïdes ou de la surdose. Les modules de formation sont accessibles sur la plateforme provinciale de l’environnement numérique d’apprentissage (ENA) (ENA, 2019). Des prétests et des post-tests de vérification des compétences sont intégrés au programme de formation en ligne. Un suivi personnalisé systémique par l’aide-infirmière de la SU est prévu en cas d’échec.
De novembre 2018 à mars 2019, les deux modules en ligne ont été privilégiés dans le plan annuel de formation par les infirmières-chefs des SU. Ces formations, offertes dans le cadre de leur temps de travail, étaient rémunérées et accompagnées d’une attestation en plus d’un crédit de formation.
Parallèlement, un module de formation complémentaire en personne de soixante minutes a été offert aux équipes des SU et aux pharmaciens d’officines avec pour thématiques : 1) l’épidémiologie des TUO ; 2) les critères et diagnostics des TUO selon le DSM-5 ; 3) les indications du TAO ; 4) la naloxone intranasale et l’induction à la B/n aux urgences ; 5) les signes d’une surdose et l’éducation préventive ; 6) le protocole pour l’induction à la B/n et ses effets indésirables y compris le sevrage provoqué (figure 2), sur le temps de travail des infirmières.
Sessions d’échange sur la mise en œuvre de l’algorithme
La mise en œuvre projetée de l’algorithme et les outils cliniques ont été présentés au personnel des SU lors des réunions d’équipe pour sensibiliser le personnel des urgences à mettre en place de nouvelles pratiques fondées sur des données probantes, promouvoir la formation continue et favoriser l’intégration rapide de l’algorithme dans leurs pratiques. À l’hôpital Notre-Dame du CIUSSS du Centre-Sud-de-l’Île-de-Montréal, les formateurs tenaient régulièrement des réunions de trente minutes en personne dans le créneau réservé à la formation SuboxED pour répondre aux questions et expliquer le nouvel algorithme à tout le personnel des SU.
Considérations éthiques
Le protocole de recherche du projet SuboxED été approuvé par le comité d’éthique pour la recherche du CHUM (MP-02-2019-7709-18.289) à titre de comité d’éthique évaluateur principal. L’autorisation d’effectuer la recherche à l’Hôpital Notre-Dame du CIUSSS Centre-Sud-de-l’île-de-Montréal et à l’Hôtel-Dieu du CIUSSS de l’Estrie-CHUS été accordée par les comités d’éthique respectifs de ces établissements. Les conseils des médecins, dentistes et pharmaciens des établissements ont révisé et approuvé les ordonnances types de naloxone et de B/n destinées aux urgences ainsi que le contenu des formations (information sur l’induction à la B/n).
Résultats de la mise en œuvre
Les résultats principaux de mise en œuvre sont présentés selon trois axes principaux à savoir : 1) description de l’intervention clinique 2) les outils cliniques 3) le nombre de professionnels de la santé formés.
Description de l’intervention
Identification des patients à RSO au SU
Lors de l’évaluation par l’infirmière au triage ou l’infirmière aux soins, l’infirmière évaluait si le patient est à RSO. Dans le cas d’une réponse positive et après avoir coché la case adéquate sur l’outil de triage, l’infirmière appliquait une étampe de couleur sur la feuille de triage. Une fois les cas identifiés, elle ou le médecin traitant utilisait une pochette spécialement créée à cet effet et disponible aux SU. Cette pochette contenait l’évaluation pour la naloxone intranasale et l’induction de la B/n. Les pochettes étaient positionnées à différents postes de travail (des médecins et des infirmiers à l’urgence ainsi que dans l’aire ambulatoire) des trois SU. De plus, lorsque le le patient ne pouvait pas être évalué par l’infirmière de triage (patient inconscient), ou selon la situation clinique, le pharmacien de l’urgence pouvait émettre un avis au dossier du patient afin de recommander la naloxone intranasale ou une évaluation pour un TAO par le médecin à l’urgence, dans un deuxième temps (annexe 2).
Pour la composante : naloxone intranasale
Si un patient était jugé à RSO, soit par un système informatisé de triage (dans le cas du CHUM), soit par triage en personne (Hôpital Notre-Dame du CIUSS du Centre-Sud-de-l’Île-de-Montréal et Hôpital Hôtel Dieu du CIUSSS de l’Estrie-CHUS), l’infirmière du triage apposait une étampe « OPIOÏDE » sur le dossier du patient. Cette étampe permettait d’alerter le médecin aux SU qui déterminait l’admissibilité du patient à recevoir la naloxone intranasale à son congé de l’urgence. Les deux doses de naloxone intranasale étaient alors remises au patient avec une courte formation faite par le personnel infirmier ou par le pharmacien au patient et une carte portefeuille créée par Santé Canada d’instructions résumant les signes de surdose aux opioïdes, les étapes d’utilisation de la naloxone et les processus d’intervention rapide en cas de surdose (annexe 3).
Pour la composante : induction à la B/n
Le triage se faisait à partir des patients identifiés à RSO. Ensuite, après une évaluation médicale, selon le diagnostic et les critères d’éligibilités, le patient pouvait recevoir ou non une prescription de la B/n (annexe 4). Les symptômes de sevrage des opioïdes étaient évalués selon l’échelle COWS (annexe 5).
Si le patient avait un TUO dont le score était > = 12 sur l’échelle COWS et qu’il présentait un sevrage modéré à sévère ou si le patient présentait les critères de TUO, un score < 12, mais n’avait pas utilisé d’opioïdes depuis un certain temps ( > = cinq jours), l’induction de la B/n pouvait débuter avec une première dose de 4 mg de la b/n sublinguale (annexe 4). Le médecin de l’urgence réévaluait ensuite le patient entre 60 et 90 minutes après induction de la B/n pour s’assurer que celle-ci ne précipite pas le sevrage. En cas de sevrage induit, le médecin à l’urgence pouvait prescrire de l’analgésie de support et contacter le médecin ayant une expertise en toxicomanies, du CHUM ou de l’hôpital Notre-Dame du CIUSS du Centre-Sud-de-l’Île-de-Montréal.
Si le patient avait un TUO et un score < 12 sur l’échelle COWS, une prescription de B/n était transmise par télécopieur à une pharmacie choisie par le patient parmi les huit pharmacies d’officine participantes au projet (annexe 1).
Si le patient ne manifestait aucun symptôme d’intoxication et qu’il avait encore des symptômes de sevrage, une dose supplémentaire de 4 mg de buprénorphine pouvait être donnée, et ce, toutes les deux heures, pour un maximum de 12 mg de buprénorphine lors des 24 premières heures.
Par la suite, le médecin de l’urgence devait rédiger la prescription puis la transmettre par télécopieur à la pharmacie d’officine partenaire choisie par le patient au congé de l’urgence. Il indiquait aussi la dose débutée à l’urgence et la dose à prendre à la pharmacie d’officine, avec des doses de buprénorphine à ajuster selon les symptômes de sevrage si nécessaire, pour un maximum total de 12 mg de buprénorphine pour les 24 premières heures (annexe 4).
Le département de l’urgence du CHUM et le département de l’hôpital Notre-Dame du CIUSSS du Centre-Sud-de-l’Île-de-Montréal donnaient un rendez-vous de suivi dans les cinq jours au SMT ou à la clinique externe du STMU selon les SU impliquées. Dans le cas de la clinique externe TAO du CIUSSS de l’Estrie-CHUS-établissement Centre Jean-Patrice-Chiasson, le rendez-vous de suivi était donné dans les sept jours suivant le congé de la SU de l’hôpital Hôtel-Dieu du CIUSSS de l’Estrie-CHUS.
Les informations de suivi après le congé de la SU (information sur la B/n, la date rendez-vous TAO et les coordonnées de la clinique TAO et de la pharmacie choisies) étaient remises aux patients.
Finalement, un médecin du SMT du CHUM était disponible 24 heures sur 24 pour répondre aux questions cliniques des médecins à l’urgence du CHUM et de l’hôpital Hôtel-Dieu CIUSSS Estrie-CHUS. Pour l’hôpital Notre-Dame du CIUSSS du Centre-Sud-de-l’Île-de-Montréal, les patients étaient dirigés vers la clinique externe du STMU. Un médecin du STMU était disponible 24 heures sur 24 pour répondre aux questions.
Outils cliniques
Le groupe de cliniciens pluridisciplinaires a conçu des outils cliniques à l’intention des professionnels des SU pour faciliter la mise en œuvre de l’algorithme de remise de naloxone chez les patients à RSO et la prescription de la B/n chez les patients ayant un TUO.
Voici la liste des outils cliniques développés :
- algorithme de prescription de la naloxone intranasale et d’induction de la buprénorphine/naloxone (figure 2) ;
- question de dépistage des patients à RSO au triage des urgences (figure 3) ;
- prescription interne de la naloxone (annexe 6) ;
- échelle clinique de sevrage des opioïdes COWS (annexe 5) ;
- prescription interne et externe de la buprénorphine/naloxone (annexe 4) ;
- enseignement au patient de la buprénorphine-naloxone (annexe 3).
Formation du personnel
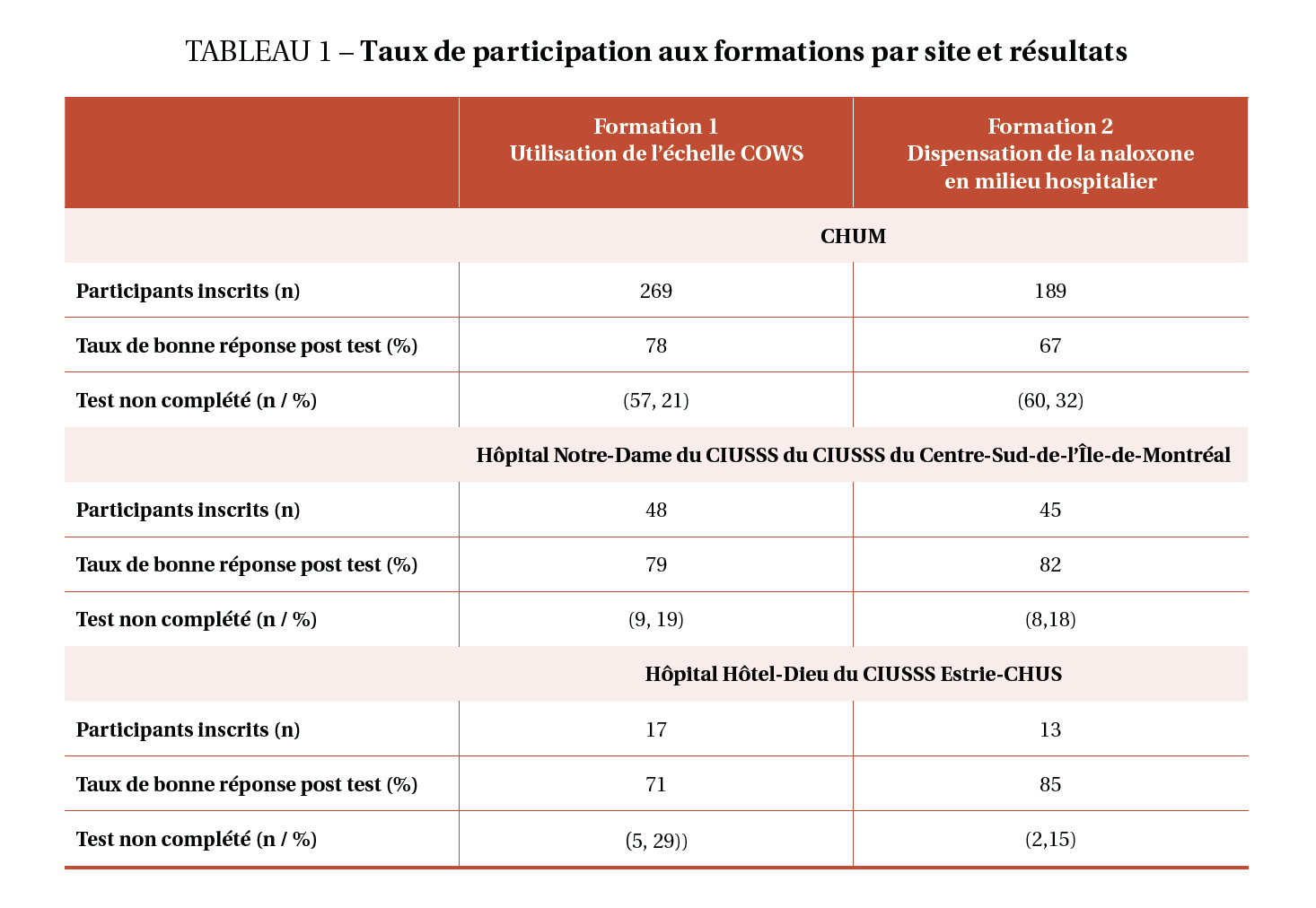
Nous avons formé 325 professionnels de la santé sur un total estimé de 400 professionnels. Ces professionnels de la santé ont suivi des modules de formations conçus par le projet SuboxED. Ces formations articulées autour de deux modules : 1) l’utilisation de l’échelle COWS entre mars 2019 et mai 2019 ; et 2) la dispensation de la naloxone en milieu hospitalier entre février 2019 et mai 2019.
Le tableau ci-après (tableau 1) résume les résultats descriptifs de nombre de participants pour chaque site.
Discussion
Ce projet témoigne du fait que la mise en œuvre de l’algorithme clinique de la remise la naloxone intranasale et de la prescription de la B/n aux SU est faisable dans le contexte québécois d’un système de santé gratuit et universel.
Défis de la mise en œuvre
De nombreux défis ont été observés dans la mise en œuvre du projet SuboxED, et ce, à chacune des étapes, parmi lesquelles : 1) l’accès sans frais à la naloxone intranasale à emporter et à la B/n en CH et leur approvisionnement ; 2) la mise en place et le maintien des formations pour le personnel selon leur disponibilité ; 3) le taux élevé de roulement du personnel des 3 SU ; 4) la capacité organisationnelle multi sites à implanter ce nouvel algorithme et l’intégrer dans leur fonctionnement et leur réalité ; 5) l’ajout d’un triage supplémentaire dans une évaluation déjà extensive pour identifier les patients RSO ; 6) les démarches administratives différentes pour chacun des deux CIUSSS et du CHUM.
La coordination des soins après le congé des urgences a nécessité une étroite collaboration entre les cliniques externes de TAO et les pharmacies d’officine. Le projet SuboxED n’est possible que si le patient peut avoir un suivi après l’induction de la B/n dans une clinique TAO après son congé de la SU dans un délai rapide (sept jours au moins dans ce projet) ; cet accès à des plages horaires rapides de cliniques TAO n’est malheureusement pas possible partout au Québec. Le SMT du CHUM offre un service de télé expertise médecine en toxicomanie, sept jours sur sept pour répondre aux questions cliniques des médecins du Québec, au-delà du projet SuboxED.
Disponibilité de la naloxone durant la mise en œuvre SuboxED
Comme précédemment mentionné, la naloxone intranasale à emporter était disponible gratuitement dans les pharmacies d’officine et les centres communautaires, via le programme PROFAN pour les personnes à RSO pour usage hors milieux cliniques.Cependant, elle ne pouvait pas être remise aux SU, car elle n’était pas couverte par la RAMQ dans les milieux hospitaliers au moment de la mise en œuvre du projet SuboxED.
Pendant l’élaboration du projet, plusieurs discussions ont eu lieu avec les représentants du MSSS, les membres du Comité national pour prévenir les surdoses aux opioïdes et plusieurs professionnels de la santé intéressés par les surdoses aux opioïdes au Québec. Avec l’appui des différents acteurs impliqués dans la prévention des surdoses aux opioïdes, le 25 octobre 2019, le MSSS a ajouté la naloxone intranasale à emporter à la liste des produits couverts par le régime d’assurance publique pour une dispensation de la naloxone pour usage hors milieu clinique aux personnes à RSO à partir d’une visite en milieu hospitalier. Ce programme de gratuité de remise de la naloxone aux personnes à RSO pour usage personnel à partir d’un milieu hospitalier explique en partie la réussite de la mise en œuvre du projet SuboxED, puisque les SU sont désormais à même d’offrir la naloxone aux patients à RSO lors d’une visite en CH pour un usage hors milieu clinique.
D’autres initiatives
Depuis la fin de SuboxED, d’autres SU au Québec ont manifesté un intérêt à intégrer un algorithme clinique inspiré par le projet SuboxED. En plus de s’inspirer des défis de la mise en œuvre de SuboxED, les SU québécoises intéressées réfléchissent à des mécanismes qui allègent et accélèrent l’intégration des outils développés et qui faciliteraient la remise de la naloxone et l’amorce de la B/n.
La deuxième phase du projet SuboxED consistera à évaluer sa mise en œuvre. L’étude effectuée évaluera l’utilisation de l’algorithme par une étude rétrospective des dossiers de patients à RSO aux SU et la satisfaction des cliniciens et des patients par une enquête. Elle permettra aussi d’évaluer le nombre de patients identifiés à RSO, le pourcentage de patients admissibles à la naloxone intranasale ou à la B/n et qui en ont reçu dans les trois SU à l’étude, le nombre de patients ayant quitté la SU avant d’avoir vu un médecin, le nombre de patients avec TAO amorcé à la SU vs en pharmacie et le niveau de satisfaction des professionnels de la santé et des patients ayant reçu la B/n.
Applicabilité de tel algorithme dans d’autres SU
Les SU desservant de plus petites populations ou en milieu rural se questionnent sur la pertinence de cet algorithme dans des milieux de soins où l’utilisation des opioïdes est moins répandue que dans les grandes villes. Or, selon l’ICIS, le taux d’intoxication aux opioïdes dans les localités plus petites est plus du double de celui observé dans les grandes agglomérations, et ce, même si la quantité d’opioïdes utilisés est moindre (ICIS, 2016). Par conséquent, toute SU gagnerait à se doter d’un algorithme de prévention active des surdoses post-séjour aux SU. Nous devons garder à l’esprit que les surdoses peuvent aussi survenir chez les patients qui reçoivent des opioïdes pour soulager la douleur, sans évidence de TUO (John et Wu, 2020).
Finalement, peu d’études ont été publiées sur la remise de la naloxone et de la prescription de B/n dans un système de soins gratuit et universel. L’étude principale de B/n aux SU est une étude dans un système de santé privé (D’Onofrio et al., 2017), qui n’inclut pas la remise de la naloxone et analyse principalement l’impact clinique d’une prescription de la B/n sur les patients ayant un TUO à travers le temps.
Conclusion
Le projet SuboxED a développé un algorithme clinique en réponse à la crise des surdoses aux opioïdes au Québec. Ce projet a été un catalyseur pour la gratuité de la naloxone à emporter aux SU au Québec. La remise de la naloxone intranasale à emporter et l’amorce et la remise de la prescription de B/n aux SU à des patients à RSO et ayant un TUO n’exigent rien de moins que la mobilisation et la volonté de tous les acteurs des SU, pharmacies d’officine et cliniques TAO. Le déploiement d’un tel algorithme dans les autres SU du Québec devrait être priorisé, tout en représentant un défi de taille. La prochaine étape du projet SuboxED consistera à évaluer l’implantation clinique dans trois SU six mois suivant l’intervention.
Annexes






Références
Agence de la santé publique du Canada. (2020). Comité consultatif spécial sur l’épidémie de surdoses d’opioïdes. Méfaits associés aux opioïdes et aux stimulants au Canada. Gouvernement du Canada. https://sante-infobase.canada.ca/mefaits-associes-aux-substances/opioides-stimulants.
American Psychiatric Association. (2013). Diagnostic and statistical manual of mental disorders (5e éd.). American Psychiatric Association. https://doi.org/10.1176/appi.books.9780890425596
Bruneau, J., Ahamad, K., Goyer, M. E., Poulin, G., Selby, P., Fischer, B., Wild, T. C. et Wood, E. (2018). Management of opioid use disorders: a national clinical practice guideline. Cmaj, 190(9), E247-E257. https://doi.org/10.1503/cmaj.170958
Busch, S. H., Fiellin, D. A., Chawarski, M. C., Owens, P. H., Pantalon, M. V., Hawk, K., Bernstein, S. L., O’Connor, P. G. et D’Onofrio, G. (2017). Cost‐effectiveness of emergency department‐initiated treatment for opioid dependence. Addiction, 112(11), 2002-2010. https://doi.org/10.1111/add.13900
Centers for Disease Control and Prevention. (2019). Life-Saving Naloxone from Pharmacies. https://www.cdc.gov/vitalsigns/naloxone/index.html
Centre hospitalier de l’Université de Montréal. (2019). Données internes des volumétries des visites annuelles à la salle d’urgence du CHUM et estimation des consultations au service de médecine de Toxicomanie (SMT) [ensemble de données inédit]. Centre hospitalier de l’Université de Montréal.
Collège des médecins du Québec, Ordre des infirmières et infirmiers du Québec et Ordre des pharmaciens du Québec. (2020). Le traitement du trouble lié à l’utilisation d’opioïdes (TUO). http://www.cmq.org/publications-pdf/p-1-2020-03-20-fr-le-traitement-du-trouble-lie-a-l-utilisation-d-opioides-tuo.pdf
Commission globale des politiques en matière de drogues. (2018). La politique en matière de drogues et le développement durable. http://www.globalcommissionondrugs.org/reports
CRAN. (2021). Prévenir et réduire les overdoses – Former et accéder à la naloxone (PROFAN). http://www.cran.qc.ca/fr/cran-centre-dexpertise/prevenir-et-reduire-les-overdoses-former-et-acceder-la-naloxone-profan
Dhalla, I. A., Mamdani, M. M., Sivilotti, M. L., Kopp, A., Qureshi, O. et Juurlink, D. N. (2009). Prescribing of opioid analgesics and related mortality before and after the introduction of long-acting oxycodone. Cmaj, 181(12), 891-896. https://doi.org/10.1503/cmaj.090784
D’Onofrio, G., Chawarski, M. C., O’Connor, P. G., Pantalon, M. V., Busch, S. H., Owens, P. H., Hawk, K., Bernstein, S. L. et Fiellin, D. A. (2017). Emergency department-initiated buprenorphine for opioid dependence with continuation in primary care: outcomes during and after intervention. Journal of General Internal Medicine, 32(6), 660-666. https://doi.org/10.1007/s11606-017-3993-2
Environnement numérique d’apprentissage provincial. (2019). Sensibilisation à l’utilisation de la trousse de naloxone en milieu intrahospitalier. Gouvernement du Québec. https://fcp.rtss.qc.ca/course/view.php?id=2276
Harris, D. S., Jones, R. T., Welm, S., Upton, R. A., Lin, E. et Mendelson, J. (2000). Buprenorphine and naloxone co-administration in opiate-dependent patients stabilized on sublingual buprenorphine. Drug Alcohol Dependence, 61(1), 85-94. https://doi.org/10.1016/s0376-8716(00)00126-5
Hoffman, K. A., Ponce Terashima, J. et McCarty, D. (2019). Opioid use disorder and treatment: challenges and opportunities. BMC Health Services Research, 19(1), 884. https://doi.org/10.1186/s12913-019-4751-4
Hôpital Notre-Dame du Centre intégré universitaire de santé et des services sociaux du Centre-Sud-de-l’Île-de-Montréal. (2019). Données internes des volumétries des visites annuelles à la salle d’urgence de l’hôpital Notre-Dame et estimation des consultations au service des toxicomanies et de médecine urbaine (STMU) [ensemble de données inédit]. Hôpital Notre-Dame du Centre intégré universitaire de santé et des services sociaux du Centre-Sud-de-l’Île-de-Montréal.
Hôpital Hôtel-Dieu du CIUSSS de l’Estrie-CHUS. (2019). Données internes des volumétries des visites annuelles à la salle d’urgence à l’hôpital Hôtel-Dieu et estimation des consultations du Centre de réadaptation en dépendance du CIUSSS de l’Estrie-CHUS [ensemble de données inédit]. Hôpital Hôtel-Dieu du CIUSSS de l’Estrie-CHUS.
Institut canadien d’information sur la santé. (2016). Hospitalisations et visites au service d’urgence liées à une intoxication aux opioïdes au Canada. https://secure.cihi.ca/free_products/Opioid%20Poisoning%20Report%20%20FR.pdf
Institut national de santé publique. (2017). Historique de l’accès à la naloxone au Québec. https://www.inspq.qc.ca/espace-itss/historique-de-l-acces-la-naloxone-au-quebec
John, W. S. et Wu, L. T. (2020). Chronic non-cancer pain among adults with substance use disorders: Prevalence, characteristics, and association with opioid overdose and healthcare utilization. Drug and Alcohol Dependence, 209, 107902. https://doi.org/10.1016/j.drugalcdep.2020.107902
Leece, P. C. C., Manson, H., Orkin, A. M., Schwartz, B., Juurlink, D. N. et Gomes, T. (2020). One-Year Mortality After Emergency Department Visit for Nonfatal Opioid Poisoning: A Population-Based Analysis. Annals of Emergency Medicine, 75(1), 20-28. https://doi.org/10.1016/j.annemergmed.2019.07.021
Mendelson J., Jones, R. T., Welm, S., Brown, J. et Batki, S. L. (1997). Buprenorphine and naloxone interactions in methadone maintenance patients. Biological Psychiatry, 41(11), 1095-1101. https://doi.org/10.1016/S0006-3223(96)00266-1
Merrall, E. L., Kariminia, A., Binswanger, I. A., Hobbs, M. S., Farrell, M., Marsden, J., Hutchinson, S. J. et Bird, S. M. (2010). Meta-analysis of drug-related deaths soon after release from prison. Addiction, 105(9), 1545–1554. https://doi.org/10.1111/j.1360-0443.2010.02990.x
Ministère de la Santé et des Services sociaux. (2018). Stratégie nationale 2018-2020 pour prévenir les surdoses d’opioïdes et y répondre. Parce que chaque vie compte. https://publications.msss.gouv.qc.ca/msss/document-002016/
National Center for Health Statistics. (2019). National Vital Statistics System, Mortality. CDC WONDER, US Department of Health and Human Services, CDC. https://wonder.cdc.gov. https://www.cdc.gov/drugoverdose/data/
National Center for Health Statistics. (2021). CDC/NCHS, National Vital Statistics
System, Mortality. CDC WONDER, US Department of Health and Human Services, CDC. https://www.cdc.gov/opioids/data/index.html
O’Brien, D. C., Dabbs, D., Dong, K., Veugelers, P. J. et Hyshka, E. (2019). Patient
characteristics associated with being offered take home naloxone in a busy, urban emergency department: a retrospective chart review. BMC Health Services Research, 19(1), 1-12.
https://doi.org/10.1186/s12913-019-4469-3
Organisation mondiale de la santé. (2014). Community management of opioid overdose. https://apps.who.int/iris/handle/10665/137462
Scholl, L., Seth, P., Kariisa, M., Wilson, N. et Baldwin, G. (2017). Drug and opioid-involved overdose deaths—United States, 2013-2017. Morbidity and Mortality Weekly Report,
67(51-52), 1419. https://doi.org/10.15585/mmwr.mm6751521e1
Stotts, A. L., Dodrill, C. L. et Kosten, T. R. (2009). Traitement de la dépendance aux
opioïdes: options en pharmacothérapie. Opinion d’expert sur la pharmacothérapie, 10(11), 1727–1740. https://doi.org/10.1517/14656560903037168
Siegel, R., S. M. H. S., Center, G. B. I., Center, P. et Links, G. W. (2019). Examining how EDs across America are addressing the opioid epidemic: Spotlight on California. ED BRIDGE. https://smhs.gwu.edu/urgentmatters/news/eds-addressing-opioid-epidemic-spotlight-ed-bridge
Tompkins, D. A., Bigelow, G. E., Harrison, J. A., Johnson, R. E., Fudala, P. J. et Strain, E. C. (2009). Validation simultanée de l’échelle de sevrage des opiacés cliniques (COWS) et des indices à élément unique par rapport à l’instrument de sevrage des opioïdes du Clinical Institute Narcotic Assessment (CINA). Dépendance aux drogues et à l’alcool, 105(1-2), 154-159. https://doi.org/10.1016/j.drugalcdep.2009.07.001
Weiner, S., Baker, O., Bernson, D. et Schuur, J. (2020). One-Year Mortality of Patients After Emergency Department Treatment for Nonfatal Opioid Overdose. Annals of Emergency Medicine, 75(1), 13-17. https://doi.org/10.1016/j.annemergmed.2019.04.020
Wesson, D. R. et Ling, W. (2003). The Clinical Opiate Withdrawal Scale (COWS). Journal
of Psychoactive Drugs, 35(2), 253-259. https://doi.org/10.1080/02791072.2003.10400007
Tous droits réservés © Drogues, santé et société, 2021












